


Fonte: https://covid19vaccinetrial.co.uk/home
Aggiornamento:
È un vaccino vettoriale, cioè la proteina del SARS-CoV-2 destinata a suscitare gli anticorpi, viene artificialmente prodotta da un adenovirus di scimpanzé. L'adenovirus è stato reso incapace di replicarsi e quindi non può dare di per sé un'infezione. Il coronavirus, sulla sua superficie, ha delle punte o spicule che contengono una glicoproteina la cui struttura è la chiave per l'invasione cellulare del virus. Gli anticorpi che si legano a questa proteina sono in grado di bloccare l'entrata del virus nelle cellule (anticorpi bloccanti). L'adenovirus utilizzato nel vaccino Oxford contiene la sequenza genica del coronavirus che contiene le istruzioni per “costruire” la proteina della spicula che viene inserita mediante tecniche di bioingegneria nell’adenovirus che di conseguenza produrrà la proteina. Questo costrutto artificiale è chiamato “piattaforma ChAdOx1”. Dopo l'inoculo nell'organismo umano, l'adenovirus vettore produce grandi quantità della proteina della spicula di SARS-CoV-2 che stimola la produzione di anticorpi.
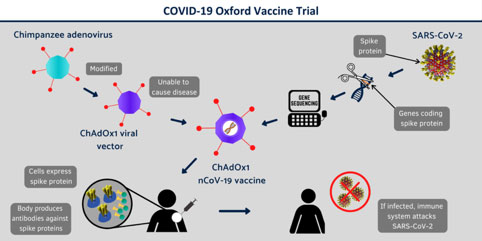
Utilizzando la piattaforma ChAdOx1 è stato precedentemente sviluppato un vaccino per un'altra malattia umana da coronavirus, cioè la sindrome respiratoria del Medio Oriente (MERS), nella quale questo vaccino ha mostrato, nei primi studi clinici, risultati promettenti.
Il reclutamento di pazienti degli studi clinici di fase I / II (COV001) è ora stato completato mentre è in corso il reclutamento per lo studio di fase II / III. Finora gli studi di ricerca clinica sono stati condotti in più sedi del Regno Unito e nei prossimi giorni verranno aggiunte altre sedi di ricerca in Brasile.
I ricercatori dei Rocky Mountain Laboratories (NIAID / NIH) hanno dimostrato che una singola dose di ChAdOx1 nCoV-19 è efficace nel proteggere il Macacus rhesus, precedentemente infettato con il coronavirus SARS-CoV-2, in piena sicurezza.
Finora, il vaccino ChAdOx1 nCoV-19 è stato somministrato a più di 320 persone e ha dimostrato di essere sicuro e ben tollerato, sebbene possa causare effetti collaterali temporanei, come aumento della temperatura, mal di testa o dolori alle braccia.
Lo studio di fase I su volontari adulti sani è iniziato ad aprile. Il 5 giugno u.s. più di 1.000 vaccinazioni erano state completate e attualmente è in corso il follow-up.
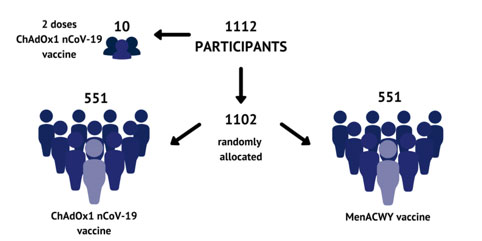
Lo studio prevede l'arruolamento di 1102 partecipanti, in più sedi di studio (Oxford, Southampton, Londra e Bristol). I partecipanti allo studio sono assegnati in modo casuale a due sottogruppi, uno che riceve il vaccino ChAdOx1 nCoV-19 e l'altro un vaccino registrato (Men ACWY), utilizzato come 'controllo' per il confronto. Il vaccino Men ACWY è un vaccino registrato contro il meningococco di gruppo A, C, W e Y che dal 2015 è somministrato abitualmente agli adolescenti nel Regno Unito per la protezione da una delle cause più comuni di meningite e sepsi. All'inizio del processo, sarà reclutato anche un piccolo gruppo separato di 10 volontari che riceveranno 2 dosi di ChAdOx1 nCoV-19 a distanza di quattro settimane. Per valutare se il vaccino è efficace contro la COVID-19, sarà fatto un confronto statistico tra il numero di infezioni nel gruppo di controllo e quello del gruppo dei vaccinati. A tal fine, è necessario che un piccolo numero di partecipanti allo studio sviluppi COVID-19.
Lo schema dello studio è il seguente:
Questo studio è attualmente in fase di partenza e si propone di valutare in che modo il nuovo vaccino ChAdOx1 nCoV-19 potrebbe proteggere dal COVID-19 le persone di una ampia gamma di età. Lo studio fornirà inoltre informazioni preziose sugli aspetti di sicurezza del vaccino e sulla sua capacità di generare un’efficace risposta immunitaria contro il virus.
In totale questo studio arruolerà fino a 10.260 adulti e bambini in tutto il Regno Unito e in Brasile.
La fase II dello studio prevede di valutare efficacia e sicurezza del vaccino ChAdOx1 nCoV-19 in persone appartenenti a fasce d'età più fragili: rispettivamente di 56-69 anni; di oltre 70 anni e la fascia pediatrica di 5-12 anni. Per questi gruppi, i ricercatori stanno valutando se esistano nella risposta del sistema immunitario.
La fase III dello studio prevede la valutazione dell’efficacia del vaccino in un gran numero di persone di età superiore ai 18 anni. Questo gruppo consentirà di valutare l'efficacia del vaccino per prevenire l'infezione da COVID-19.
I partecipanti adulti in entrambi i gruppi di Fase II e Fase III saranno randomizzati a ricevere una o due dosi del vaccino ChAdOx1 nCoV-19 o di un vaccino registrato (Men ACWY) che verrà utilizzato come 'controllo' per il confronto. Per valutare se il vaccino protegge dalla COVID-19, si farà una valutazione statistica di confronto tra il numero di infezioni nel gruppo di controllo e il numero di infezioni nel gruppo dei vaccinati con ChAdOx1 nCoV-19. A tal fine, è necessario che un piccolo numero di partecipanti allo studio sviluppi COVID-19. La rapidità, con cui saranno raggiunti i numeri richiesti per un risultato definitivo, dipenderà dai livelli di trasmissione dei virus nella comunità. Se la trasmissione del contagio rimane elevata, si potranno ottenere abbastanza dati sulla efficacia del vaccino in un paio di mesi, ma se i livelli di trasmissione diminuissero, ciò potrebbe richiedere fino a 6 mesi. Nel tentativo di acquisire i dati di efficacia con la maggiore velocità possibile, sarà data la priorità all’arruolamento di coloro che hanno maggiori probabilità di essere esposti al virus SARS-CoV-2, come gli operatori sanitari in prima linea, il personale di supporto in prima linea e gli operatori sanitari che operano sul territorio nel settore pubblico.
Contemporaneamente alla preparazione e allo svolgimento del primo studio clinico, la produzione del vaccino viene potenziata in modo che possa essere utilizzata per studi più ampi e per il potenziale utilizzo futuro.
AstraZeneca sta collaborando con un numero di paesi e organizzazioni multilaterali per rendere il vaccino dell'Università di Oxford ampiamente accessibile in tutto il mondo, in modo equo. AstraZeneca ha ricevuto il 21 maggio 2020 oltre 1 miliardo di dollari dalla US Biomedical Advanced Research and Development Authority (BARDA) per lo sviluppo, la produzione e la consegna del vaccino, a partire dall'autunno 2020. Italia, Germania, Francia, e Olanda, che hanno fatto fronte comune per negoziare con potenziali produttori e aziende farmaceutiche l’acquisto anticipato di vaccini per COVID-19, hanno stipulato in questi giorni un contratto anticipato con Astra Zeneca per l’acquisto anticipato del vaccino ChAdOx1 nCoV-19.
